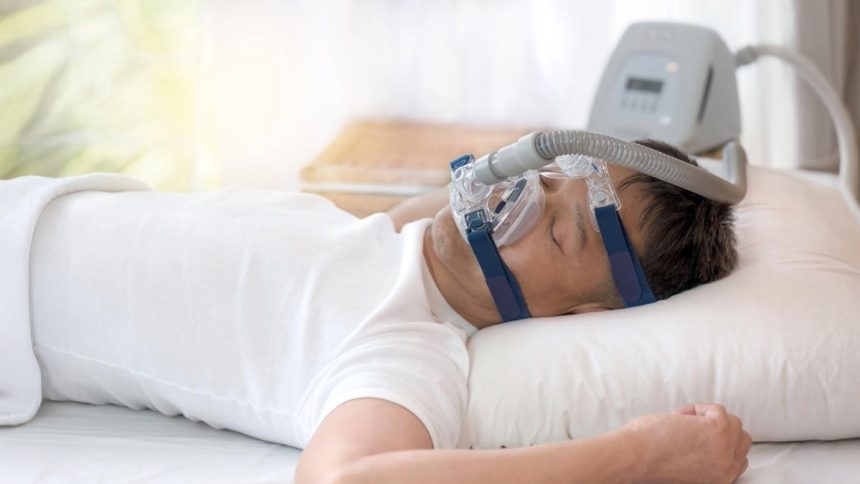
Un espoir pour les 1,6 million de Français concernés : le médicament AD109, développé par la start-up Apnimed, pourrait bientôt offrir une alternative au masque PPC, longtemps incontournable dans le traitement de l’apnée du sommeil.
Une alternative médicamenteuse attendue
L’apnée obstructive du sommeil, qui se manifeste par des arrêts respiratoires répétés durant la nuit, est plus qu’un simple trouble du sommeil : elle affecte la qualité de vie, le cœur, et le cerveau. Le traitement de référence, la pression positive continue (PPC), reste efficace, mais son port nocturne s’avère inconfortable pour de nombreux patients, qui finissent par l’abandonner.
Un nouveau traitement prometteur, l’AD109, suscite donc de grands espoirs. Ce médicament oralcombine deux molécules déjà connues : l’une agit en stimulant les muscles du pharynx, l’autre empêche leur relâchement. Résultat : la respiration reste fluide, et les apnées se réduisent.
Des résultats cliniques encourageants
Testé sur 646 patients, l’AD109 affiche des résultats très prometteurs :
• 56 % des patients traités ont constaté une nette amélioration de leurs symptômes.
• 22 % ont vu leur apnée totalement résolue.
• Les effets secondaires, modérés, se limitent à une sécheresse buccale et quelques insomnies chez un quart des participants.
Selon le Dr Maxime Patout, pneumologue à l’hôpital de la Pitié-Salpêtrière, ce traitement pourrait convenir aux patients ne tolérant pas la PPC, notamment dans les cas modérés.
Un enjeu de santé publique
L’apnée du sommeil est souvent sous-estimée. Elle provoque une hypoxie intermittente (manque d’oxygène temporaire), ce qui augmente les risques de :
1. Maladies cardiovasculaires (AVC, infarctus).
2. Hypertension chronique.
3. Troubles de la mémoire et de l’humeur.
4. Diminution de l’espérance de vie.
Un traitement plus simple à administrer pourrait donc éviter bien des complications et améliorer l’observance thérapeutique.
Vers une autorisation en 2026 ?
Apnimed prévoit de finaliser un second essai clinique à grande échelle d’ici l’été 2025. Si les résultats se confirment, une demande d’autorisation auprès de la FDA (Agence américaine des médicaments) pourrait être déposée en 2026.
L’AD109 ne remplacera sans doute pas immédiatement la PPC, notamment dans les cas sévères, mais il pourrait changer la donne pour des milliers de patients en quête de confort.
La Rédaction